Pada
gambar (a), kedua bejana diisi dengan zat cair yang sejenis dan
dipanaskan dalam selang waktu yang sama. Ternyata pada bejana yang
berisi zat cair lebih sedikit, suhunya lebih tinggi. Jadi, jumlah kalor
yang diserap benda berbanding lurus dengan massa benda ( Q ∞ m).
Pada gambar (b), kedua benda diisi zat cair yang sejenis dan sama
massanya. Ternyata pada selang waktu yang sama, bejana yang dipanasi
dengan api lebih besar, memiliki suhu yang lebih tinggi. Jadi, jumlah
kalor sebanding dengan kenaikan suhu (Q ∞∆T). Pada gambar (c),
bejana A diisi dengan alkohol dan bejana B diisi dengan air. Massa
kedua zat cair di dalam masing-masing bejana sama. Ternyata dalam selang
waktu yang sama, suhu termometer pada bejana A lebih tinggi daripada
termometer pada bejana B. Kalor jenis alkohol lebih kecil daripada kalor
jenis air. Jadi, kalor sebanding dengan kalor jenis (Q ∞ c)
Berdasarkan
kesimpulan di atas, jumlah kalor yang diserap atau dilepas suatu benda
dapat dirumuskan dalam persamaan sebagai berikut.
Q = m c ∆T
Keterangan:
Q = jumlah kalor
m = massa zat
c = kalor jenis
∆T = kenaikan suhu 0C.
Kalor jenis benda adalah banyaknya kalor yang diperlukan tiap 1 gram zat untuk menaikkan suhunya sebesar 1. Contohnya, kalor jenis air adalah 4200 J/kg0C, artinya untuk memanaskan suhu 1 kg air sebesar 10C, diperlukan energy sebasar 4200 J. Untuk zat yang jenisnya sama, berarti juga memiliki kalor jenis
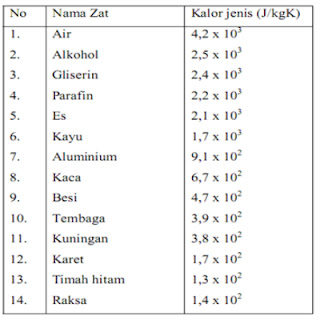
yang sama besar. Perhatikan nilai kalor jenis berbagai benda pada tabel di bawah ini.
Tabel 1 Kalor jenis beberapa zat
Selain kalor jenis, dikenal pula besaran kapasitas pada konsep kalor.
Kapasitas kalor (C) adalah banyaknya kalor yang diperlukan zat untuk menaikkan suhunya sebesar 10C.
Untuk zat yang sejenis, belum tentu memiliki kapasitas kalor yang sama.
Secara matematis, kapasitas kalor dirumuskan sebagai berikut:
Q = m c ∆t
C= m.c
Satuan kapasitas kalor adalah J/K.

Komentar
Posting Komentar