NERACA MASSA (Neraca Bahan)
October 3, 2009 I. PendahuluanNeraca massa merupakan perincian banyaknya bahan-bahan yang masuk, keluar dan menumpuk dalam suatu alat pemroses. Perhitungan dan perincian banyaknya bahan-bahan ini diperlukan untuk pembuatan neraca energi, perhitungan rancangan dan evaluasi kinerja suatu alat atau satuan pemroses. Untuk rancangan misalnya, diperlukan perhitungan jumlah hasil yang akan diperoleh atau sebaliknya bahan baku dan bahan pembantu yang diperlukan untuk mendapatkan hasil dalam jumlah tertentu. Jumlah energi atau panas yang diperlukan bergantung pada jumlah bahan yang diproses. Demikian juga ukuran peralatan, ditentukan jumlah bahan yang harus ditangani.
II. Prinsip Neraca Bahan
Neraca massa merupakan penerapan hukum kekekalan massa terhadap suatu proses. Massa jumlahnya tetap, tidak dapat diciptakan maupun dimusnahkan. Prinsip ini tidak berlaku bagi proses yang menyangkut reaksi-reaksi inti(nuklir). Pada reaksi ini terjadi pemusnahan massa dan berubah menjadi energi. Hubungan antara jumlah massa yang musnah dan energi yang timbul diberikan dalam rumusan Einstein yang terkenal yaitu :
E = m . c2
E = Jumlah energi yang timbul, erg
m= jumlah massa yang musnah, gram
c = kecepatan cahaya = 3 x 1010 cm/detik
III.Proses Batch dan Proses Berkesinambungan
Di dalam industri proses dapat dilaksanakan secara batch (per angkatan) dan secara berkesinambungan. Pada proses batch pemasukan reaktan dan pengeluaran hasil dilakukan sekali-sekali dalam selang waktu tertentu. Contoh proses batch adalah proses memasak makanan di rumah. Pemanasan suatu cairan dalam tanki dengan steam yang dialirkan dalam jaket Gambar (a) merupakan contoh proses batch.
(b). Proses Berkesinambungan.
Proses berkesinambungan banyak dilakukan dalam industri. Bahan dimasukkan dan hasil dikeluarkan secara berkesinambungan (terus menerus dengan laju tertentu). Dalam bagan di bawah ini adalah contoh proses pemanasan suatu cairan secara berkesinambungan.
Cairan A secara tetap mengalir terus menerus memasuki alat penukar panas. Steam pemanas juga dimasukkan terus menerus.
IV. Persamaan Neraca Massa
Neraca massa dibuat untuk suatu alat atau unit dengan batasan tertentu. Bahan- bahan yang perlu diperinci banyaknya adalah bahan-bahan yang masuk dan keluar batasan yang ditetapkan.
Berdasarkan hukum kekekalan massa, banyaknya bahan yang masuk, keluar dan menumpuk dalam sistem yang batasnya telah kita tetapkan, berlaku hubungan berikut :
Jumlah massa masuk – jumlah massa keluar = Jumlah massa yang menumpuk di dalam batas sistem
Ri – Ro = A
Persamaan ini dapat ditetapkan pada proses berkesinambungan dengan mendasarkan perhitungan pada suatu jangka waktu tertentu yang kita pilih
(misalnya : 1 jam, 1 hari, 1 menit).
Dalam hal masukan atau keluaran berupa campuran berkomponen banyak, neraca massa dibuat untuk massa keseluruhan dan untuk masing-masing komponen.
V. Keadaan mantap (steady) dan Tak mantap (unsteady)
Proses dalam keadan mantap (steady) adalah proses dimana semua aliran yang masuk dan keluar, laju dan komposisinya tetap (tidak bergantung dari waktu). Pada keadaan seperti ini jumlah massa yang menumpuk juga tetap (laju akumulasi/penumpukan = 0 ) dan tidak turut diperhitungkan. Pada keadaan ini persamaan neraca massa menjadi :
Jumlah massa masuk = Jumlah massa keluar
Pada proses yang tidak/belum mantap (unsteady/transisi), laju alir maupun komposisi senantiasa berubah (merupakan fungsi waktu). Untuk keadaan ini akumulasi selalu diperhitungkan.
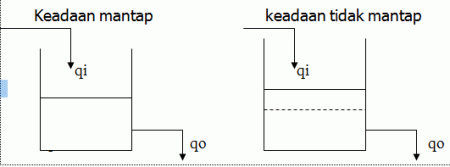
pada keadaan mantap :
qi = qo = tetap
tinggi permukaan tetap
qi = qo = q (t), fungsi waktu (t)
tinggi permukaan berubah
VI. Langkah-langkah Pembuatan Neraca Massa (Bahan)
Harus diketahui terlebih dahulu apakah proses berlangsung secara mantap atau tidak. Apabila proses tidak menyangkut reaksi kimia, neraca bahan dapat dibuat dengan satuan-satuan kg, lb, kmol dsb. Dalam hal ada reaksi kimia, sebaiknya dipakai satuan mol karena zat-zat bersangkutan secara stoikhiometri.
Untuk memudahkan perhitungan neraca massa diambil langkah-langkah sbb :
1. Buat diagram proses (block diagram)
2. Tuliskan besaran, data yang diketahui dan diperlukan pada diagram tersebut.
3. Tuliskan persamaan reaksi kimianya.
4. Tetapkan dasar perhitungan.
Semua perhitungan bahan (total maupun untuk masing-masing komponen) harus dilakukan pada dasar yang sama. Dasar perhitungan dapat berupa sejumlah massa aliran tertentu atau jangka waktu tertentu.
5. Buat persamaan neraca massa (keseluruhan dan komponen-komponen yang diperlukan.
6. Selesaikan persamaan-persamaan neraca bahan tersebut.
VII. Penyelesaian Neraca Bahan Pada Keadaan Mantap(steady)
Berdasarkan jenisnya persoalan neraca bahan dapat diselesaikan dengan cara berikut :
1. Secara langsung
2. Secara aljabar
3. Secara langsung atau aljabar dengan bantuan komponen penghubung ( tie component ).
Penyelesaian Secara Langsung :
Penyelesaian secara langsung dapat dilakukan bila hanya satu besaran atau satu komponen yang tidak diketahui.
Contoh soal :
Suatu bahan basah dengan kandungan air 60% dikeringkan sampai 75% airnya menguap. Hitunglah :
a.Komposisi akhir bahan
b. Jumlah air yang diuapkan tiap kg bahan basah.
Penyelesaian :
Dasar perhitungan : 100 kg bahan basah
Air dalam bahan, mula-mula = (0,6) (100) = 60 kg
Air menguap = (0,75) (60) = 45 kg
Air sisa di dalam bahan = 60 – 45
= 15 kg
Maka a). Komposisi akhir bahan :
Bahan kering = 40 kg
Air = 15 kg
Total 55 kg
b). Kandungan air = 15 / 55 x 100% = 27,3%
Penyelesaian Menggunakan Metode Aljabar :
Pada pemecahan secara langsung, bilangan yang tidak diketahui hanya pada satu aliran. Pemecahan bisa langsung dengan penambahan atau pengurangan. Pada cara aljabar, bilangan yang tidak diketahui lebih dari 1. Yang tidak diketahui diumpamakan dengan suatu huruf. Kalau sistem terdiri dari beberapa peralatan, neraca dibuat untuk tiap alat. Neraca untuk seluruh sistem adalah jumlah neraca tiap alat. Memecah problem besar menjadi kecil lebih memudahkan perhitungan, bisa dilakukan neraca terhadap titik pencampuran (= pertemuan 3 atau lebih aliran).
Komentar
Posting Komentar